本文對界面現(xiàn)象的簡要介紹,旨在幫助界面測量技術(shù)的使用者更好地了解哪種儀器最適合于某一問題,以及了解測量數(shù)據(jù)存在哪些可能性。
界面研究的動機有很多。許多應(yīng)用是基于泡沫或乳劑。作為一個例子,乳化液系統(tǒng)的原理特征如下圖所示。
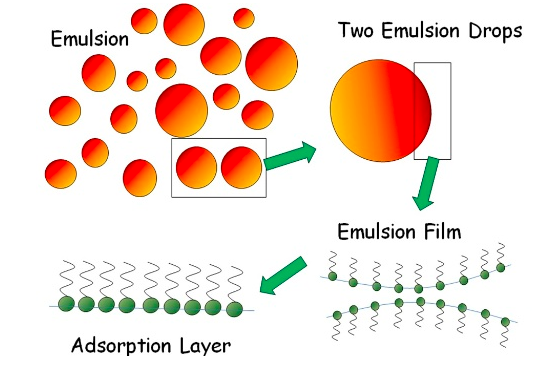
乳劑是由大量不同大小的液滴相互作用而成的。當兩滴水滴相互接觸時,形成一個液體膜,被吸附的分子穩(wěn)定下來,這里用被吸附的表面活性劑表示。這種薄膜是由兩個吸附層構(gòu)成的。因此,這些吸附層的性質(zhì)也受到壓縮、膨脹或剪切等變形的影響,對于理解乳劑的形成和穩(wěn)定至關(guān)重要。泡沫的情況與乳劑有很多相似之處,也會出現(xiàn)類似的問題。
吸附的表面活性劑
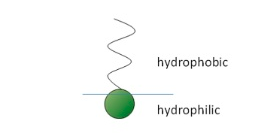
表面活性劑是一種具有兩親性的分子,即它們由親水部分和疏水部分組成。親水的頭基傾向于位于水中,而疏水的尾巴傾向于位于空氣或油中,這使得界面成為這種兩親分子的理想位置。
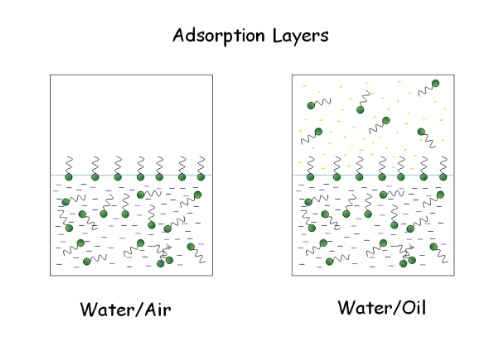
吸附層的關(guān)鍵參數(shù)是其形成過程中的吸附動力學、吸附平衡參數(shù)和流變行為,包括擴張和剪切的彈性和粘度(在寬頻率區(qū)間)。在水和油等兩種不混溶液體的界面上,分子吸附并部分進入油相。表面活性劑在兩相間的分布由分布系數(shù)給出。
等溫吸附
表面活性劑或蛋白質(zhì)的表面活性最好用所謂的吸附等溫線來證明。這個等溫線表示體濃度c和界面上的表面過度γ(吸附)之間的關(guān)系。最簡單的關(guān)系是線性亨利等溫線:
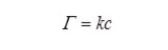
最常用的等溫線,然而,是Langmuir等溫線,它包含兩個物理參數(shù),一個特征濃度a(界面一半被表面活性劑覆蓋),以及可以吸附到γ∞的最大數(shù)量

下面的示意圖顯示了在溶液體中,γ如何隨著濃度c的增加而變化
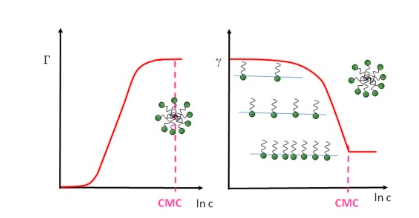
當表面活性劑達到一定體積濃度時,表面被完全覆蓋,不再有分子被吸附在界面上,進一步的表面活性劑分子在溶液體積中形成聚集體,即膠束。在這個所謂的臨界膠束濃度CMC下,γ基本上變成常數(shù),而表面張力也有一個扭結(jié),在CMC以上幾乎保持不變。
平衡吸附測定方法
橢圓測量術(shù)是一種直接測量表面活性劑在液界面吸附的方法。關(guān)于其優(yōu)缺點和適用范圍,請查閱文獻(H. Motschmann and R.Teppner, Ellipsometry, in “Novel Methods to Study Interfacial Layers”, Studies in Interface Science, Vol. 11, D. M?bius and R. Miller (Eds.), Elsevier, Amsterdam, 2001, p. 1)比較容易理解的是溶液的表面張力。通過熱力學模型,可以從所謂的表面張力-濃度等溫線g(c)確定吸附量。與上述Langmuir等溫線等價的是von Szyszkowski等溫線:
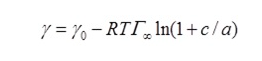
這里g0為純?nèi)軇┑谋砻鎻埩?,R和T為氣體低常數(shù)和絕對溫度。
經(jīng)典等溫線,如Langmuir等溫線,以及更先進的Frumkin等溫線,并不能完美地描述所有的實驗數(shù)據(jù)。最近,更好的模型被開發(fā)出來,并被總結(jié)在一本書中(V.B. Fainerman, D. M?bius and R. Miller (Eds.), Surfactants – Chemistry, Interfacial Properties and Application, in Studies in Interface Science, Vol. 13, Elsevier, 2001 )如下圖所示為經(jīng)典表面活性劑模型脂肪酸系列的5個成員的表面張力等溫線。
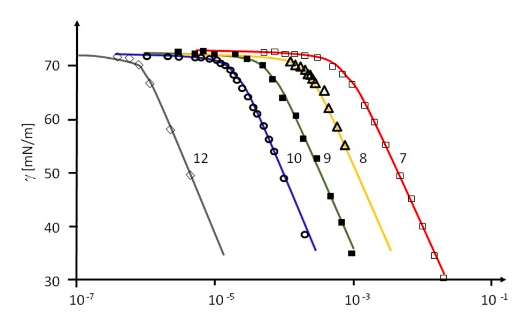
吸附動力學
表面活性分子在界面處的吸附過程是一個時間過程。當形成新的界面時,沒有分子被吸附??拷缑娴膶涌梢允紫任?,在界面附近的層中產(chǎn)生濃度梯度。由于擴散作用,分子在溶液體中移動并重新建立均勻分布。下面的示意圖顯示了這種吸附過程的步驟。
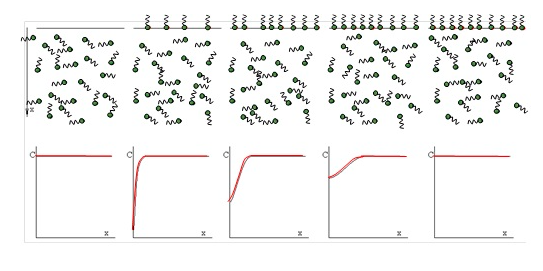
圖中顯示了表面的濃度梯度如何隨著時間的推移先增加后減少,最終導致表面活性劑在溶液體積中再次均勻分布。描述表面活性劑在溶液表面的“擴散控制”吸附過程的理論模型由Ward & Tordai于1946年導出,并得到了一個伏特拉型積分方程:

式中D為擴散系數(shù),co為表面活性劑體積濃度。這個方程描述了γ(t)隨時間t的變化,然而,它在動態(tài)表面張力數(shù)據(jù)g(t)中的應(yīng)用并不簡單。在上面由Fainerman, Mobius和Miller提到的書中,a段落致力于所有吸附動力學模型的一般物理思想,以及各種模型的特殊性。
動態(tài)表面張力與重疊的時間間隔
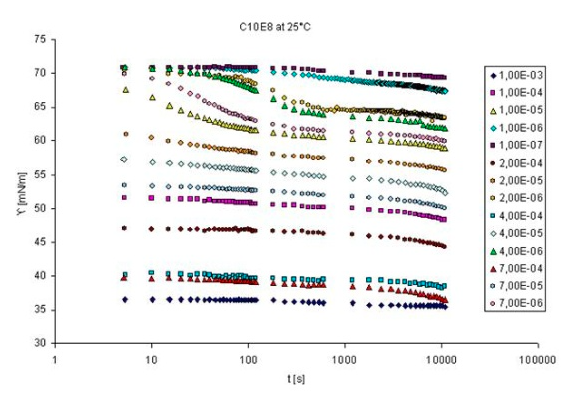
這種方法產(chǎn)生很長吸附時間(這里高達10.000秒),然而,短時間內(nèi)沒有數(shù)據(jù)提供這種技術(shù)。對于7×10-6 mol/l的濃度,這個時間間隔似乎足夠了,對于更高的濃度,然而,表面張力在5秒(PAT-1M測得的最低時間在這里,實際上可以從1秒左右開始),由于吸附顯著降低。由于吸附作用而顯著降低。對于這種表面活性劑濃度的測量需要更短的吸附時間。在吸附時間低至1ms甚至更短的情況下,唯一能提供數(shù)據(jù)的技術(shù)是氣泡壓力張力測定法(參見SINTERFACE的BPA-1S和BPA-2S)。對于動態(tài)界面張力,像1ms這樣的短吸附時間用現(xiàn)有的任何方法都無法達到。下面的示意圖概述了現(xiàn)有的動態(tài)表面和界面張力的方法以及相應(yīng)的時間窗口。降壓模塊(DPA-1和ODBA-1)是第一個實驗裝置,它允許在較短的吸附時間內(nèi)進行測量。根據(jù)實驗細節(jié),甚至低于10毫秒的時間都可以訪問。
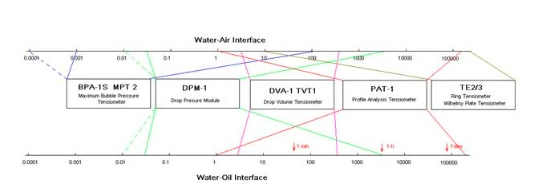
選擇一種合適的方法有時并不容易,因為對于某些問題,存在著許多方法,并且所有這些方法在易于操作、可用的溫度控制、適用于液-氣和液-液界面等方面都有其他方法的優(yōu)勢。然而,同樣明顯的是,沒有一種方法能夠涵蓋所有的時間和需求范圍。注意,對于濃度較高的溶液,即CMC以上的表面活性劑溶液,即使100μs也會出現(xiàn)較長的吸附時間。一份使用液滴和氣泡方法的實驗可能性的實際總結(jié)和一個極好的實驗例子選擇已經(jīng)發(fā)表了最近(R. Miller and L. Liggieri (Eds.), Bubble and Drop Interfaces, in “Progress in Colloid and Interface Science”, Vol. 2, Brill Publ., Leiden, 2011, ISBN 978 90 04 17495 5).





